Общее описание
Титановый порошок – мелкодисперсная фракция, состоящая из зерен заданной формы, размера и химического состава (рис. 1).

Рисунок 1. Титановый порошок
Порошок можно считать основой основ в процессе получения различных изделий из титана. Это один из важнейших элементов в цепочке создания титановой продукции, от структуры, свойств и характеристик которого во многом зависят параметры получаемых изделий. Порошки титана, вне зависимости от их структурного состава и методов получения, обладают всеми базовыми полезными свойствами данного металла, включая:
- устойчивость к коррозии;
- твердость;
- пористость;
- пластичность;
- термостойкость;
- механическую прочность;
- способность к спеканию и свариваемости;
- легкость;
- износостойкость;
- хорошие показатели прессуемости.
Продукцию различают по весу, насыпной плотности, способности к спеканию, химическому и гранулометрическому составу, марке, способу получения.
Композиционные титановые порошки, помимо базовых свойств основного компонента (Ti), обретают также полезные характеристики входящих в их состав легирующих элементов.
Основные стандарты, марки, требования к качеству
Сообразно способу изготовления и свойствам титановые порошки подразделяются на четыре основных типа, регламентируемых соответствующими стандартами.
ТУ1791-449-05785388-2010 «Титан пористый, порошок. Технические условия»
Действие данного стандарта распространяются на категорию титановых пористых порошков (ТПП), создаваемых методом измельчения (размола) титановой губки. Порошки ТПП получают, главным образом, перерабатывая отсевы губчатого титана с применением способа гидрирования-дегидрирования.
Порошки ТПП, с учетом размерных параметров зерен и химсостава, подразделяются на восемь марок (табл. 1).
Таблица 1. Марки, фракционные показатели и химсостав порошков ТПП
| Фракц., мм | Масс. доля фракции, не менее | Химсостав, % | ||||
|---|---|---|---|---|---|---|
| Ti | Масс. содерж. примесей | |||||
| Fe | N | Cl | ||||
| ТПП-1 | -5+0 | 80 | Базис | 1,8 | 0,30 | 0,30 |
| ТПП-2 | -3,2+0 | 80 | Базис | 1,8 | 0,30 | 0,30 |
| ТПП-3 | -3,2+1,0 | 80 | Базис | 0,4 | 0,08 | 0,10 |
| ТПП-4 | -1,0+0 | 80 | Базис | 1,0 | 0,20 | 0,20 |
| ТПП-5 | -1,0+0,63 | 70 | Базис | 0,5 | 0,15 | 0,15 |
| ТПП-6 | -0,63+0,306 | 65 | Базис | 0,8 | 0,25 | 0,25 |
| ТПП-7 | -0,306+0,16 | 60 | Базис | 1,1 | 0,50 | 0,45 |
| ТПП-8 | -0,16 | 60 | Базис | 2,1 | 1,10 | 0,50 |
Частицы порошков ТПП могут обладать чешуеобразной, игольчатой либо округлой (овальной) формой. Для порошков, имеющих овальную форму зерен, обозначение марки дополняется буквенным символом «А», напр. ТПП-ЗА.
Как видно из приведенной таблицы, данные порошки отличает высокое содержание основных примесей. Фактор насыщенности порошков ТПП примесями значительно сужает спектр их использования в высокотехнологичных производственных процессах в сравнении с порошками Ti, изготавливаемыми прочими способами.
Из порошков ТПП изготавливают, главным образом, тугоплавкие титановые композиции и спеченные изделия, они находят применение и в некоторых других производственных процессах.
ТУ 14-22-57-92 «Порошок титановый»
Действие стандарта охватывает, в частности, категорию титановых порошков, получаемых путем восстановления двуокиси титана (TiO2) гидридом кальция (СаН2) в гидрид титана (TiH2) и разложением последнего на Н и Ti (дегидрирование).
Порошки, получаемые в рамках данного стандарта, в зависимости от содержания примесей и их массовой доли, имеют следующую маркировку (табл. …):
Таблица 2. Марки порошков Ti и требования к их качеству согласно ТУ 14-22-57-92
| Марка порошка | Массовая доля, %, не более | ||||||
|---|---|---|---|---|---|---|---|
| N | C | H | Fe, Ni | Si | Ca | Cl | |
| ПТК-1 | 0,07 | 0,05 | 0,35 | 0,35 | 0,10 | 0,08 | 0,003 |
| ПТК-2 | 0,20 | 0,05 | 0,35 | 0,35 | 1,00 | 0,08 | 0,003 |
| ПТC-1 | 0,08 | 0,05 | 0,35 | 0,40 | 0,10 | 0,08 | 0,004 |
| ПТC-2 | 0,20 | 0,05 | 0,35 | 0,40 | 1,00 | 0,08 | 0,004 |
| ПТМ-1, ПТМ-2 | 0,08 | 0,05 | 0,35 | 0,40 | 0,10 | 0,08 | 0,004 |
| ПТМ(А)-2, ПТМ-3 | 0,08 | 0,05 | 0,35 | 0,40 | 0,10 | 0,05 | 0,004 |
| ПТМ(А)-3 | 0,20 | 0,05 | 0,35 | 0,40 | 1,00 | 0,08 | 0,004 |
| ПТОМ-1 | 0,08 | 0,05 | 0,40 | 0,40 | 0,10 | 0,08 | 0,004 |
| ПОМ-2 | 0,20 | 0,05 | 0,40 | 0,40 | 1,00 | 0,08 | 0,004 |
| ГТ | - | - | Не менее 3,5 | - | - | - | - |
Порошки Ti и его сплавов, производимые данным способом, имеют иррегулярную (неправильную) форму зерен и развитую поверхностную структуру (рис. 2). Поэтому они хорошо поддаются формовке при относительно невысоких показателях пресс-давления как в жестких матричных емкостях, так и в эластичных контейнерах (способ гидростатического прессования).

Рисунок 2. Структура зерен титановых порошков, изготавливамых восстановлением в рамках ТУ 14-22-57-92
Такие порошки востребованы для производства компонентов часов и электронных приборов. С их помощью также производят фильтры для обеззараживания воды и воздуха, устранения механических включений. Кроме того, порошки, изготавливаемые в рамках данного стандарта, часто используются в пиротехнической сфере.
ТУ 48-10-78-83 с 7 изменениями «Порошок титановый химический»
Порошок титановый химический (ПТХ), изготавливаемый по этому стандарту, получают из губчатого Ti с применением механохимического, термохимического (металлотермия) и плазмохимического методов.
В зависимости от химсостава, размерности и твердости зерен по Бринеллю порошки ПТХ выпускаются четырнадцати марок (табл. …), где аббревиатура ПТХ обозначает общее название («Порошок титановый химический»), 1-я цифра отображает тип (НВ) порошка по величине частиц, а вторая – по показателю НВ.
Таблица 3. Марки порошков титановых химических и требования к их качеству
| Марка | Фракции, мм | Отклонение от нормы, %, не более | Массовая доля примесей, %, не более | ||||
|---|---|---|---|---|---|---|---|
| крупнее | мельче | Fe | Cl | N | H | ||
| ПТХ-1-1 | -3,0+1,0 | 10 | 10 | 0,3 | 0,06 | 0,05 | 0,1 |
| ПТХ-1-2 | -3,0+1,0 | 10 | 15 | 0,8 | 0,07 | 0,08 | 0,2 |
| ПТХ-2-1 | -1,0+0,63 | 10 | 10 | 0,3 | 0,06 | 0,05 | 0,1 |
| ПТХ-2-2 | -1,0+0,63 | 10 | 15 | 0,8 | 0,08 | 0,08 | 0,2 |
| ПТХ-3-1 | -1,0+0,18 | 10 | 10 | 0,3 | 0,07 | 0,05 | 0,1 |
| ПТХ-3-2 | -1,0+0,18 | 10 | 15 | 0,8 | 0,09 | 0,08 | 0,2 |
| ПТХ-4-1 | -0,63+0,18 | 10 | 10 | 0,4 | 0,08 | 0,08 | 0,1 |
| ПТХ-4-2 | -0,63+0,18 | 10 | 15 | 0,9 | 0,09 | 0,08 | 0,3 |
| ПТХ-5-1 | -0,45+0,18 | 10 | 10 | 0,8 | 0,10 | 0,10 | 0,4 |
| ПТХ-5-2 | -0,45+0,18 | 10 | 15 | 1,0 | 0,12 | 0,12 | 0,6 |
| ПТХ-6-1 | -0,18 | 15 | - | 0,8 | 0,09 | 0,08 | 0,2 |
| ПТХ-6-2 | -0,18 | 30 | - | 1,8 | 0,10 | 0,20 | 0,5 |
| ПТХ-7-1 | -0,18 | 15 | - | 0,9 | 0,09 | 0,08 | 0,5 |
| ПТХ-6-2 | 30 | - | 1,8 | 0,10 | 0,20 | 0,9 | |
Порошки ПТХ применяют, главным образом, для изготовления конечной продукции способами порошковой металлургии.
ТУ 48-10-22-85 «Порошок титановый электролитический. Технические условия»
Для получения порошков титана электролитических (ПТЭ) применяют метод электролиза солевых расплавов. Их характерное отличие – незначительная доля примесей, в особенности O и N.
Сообразно гранулометрическому составу к основному названию марки добавляют символы К (крупный), С (средний) и М (мелкий). Цифровые обозначения 0 1 2 после буквенной аббревиатуры обозначают группы в зависимости от состава и твердости по Бринеллю. Конфигурация зерен – дендритная, пластинчатая или осколочная.
Порошки ПТЭ наиболее пластичны. Их характеризует минимальная усадка в ходе спекания, что обеспечивает возможность получения изделий, имеющих высокую плотность. Свойства ПТЭ возможно регулировать в широком диапазоне за счет изменения параметров электролиза.
Производственные технологии
Выбор производственных технологий изготовления титановых порошков обусловлен широким применением получаемой из них продукции в различных хозяйственных отраслях. При этом свойства порошкообразного Ti и его сплавов могут изменяться в широком функциональном диапазоне и зависят от способа получения. Что, в свою очередь, позволяет изготавливать продукцию промышленными партиями.
На сегодняшний день разработано большое количество технологических схем изготовления порошков на титановой основе.
К наиболее значимым из них можно отнести:
- измельчение компактного Ti (в т.ч. с применением способа гидрирования-дегидрирования);
- восстановление диоксида титана (TiO2) с помощью гидрида кальция (СаН2) в гидрид титана (TiH2) и разложение последнего на Н и Ti (гидрирование-дегидрирование).
- способ металлотермического восстановления с помощью Mg или Na из четыреххлористого титана (TiCl4);
- электролиз расплавов солей Ti.
Рассмотрим перечисленные производственные технологии получения титанового порошка более подробно.
Механический способ изготовления порошков из пористого Ti (ТПП)
Простейшей и самой малозатратной технологией получения пористого порошка Ti (ТПП по ТУ1791-449-05785388-2010) является измельчение и сепарация титанового сырья губчатой структуры. Титановая губка имеет вид рыхлой пористой массы, получаемой из концентрата ильменитовых руд и способной активно адсорбировать пары воды, кислород и азот.
Процесс измельчения осуществляется в специальных мельницах-дробилках (рис. 3).

Рисунок 3. Мельница для губчатого титана
Однако сам по себе размол без дополнительных операций не способен обеспечить получение порошка с зернами правильной формы. Между тем, порошки, в которых частицы имеют правильную форму, лучше спекаются, а полученные из них изделия отличаются сочетанием полезных функциональных качеств, и прежде всего – долговечностью. Поэтому для выпуска высококачественных порошков требуемой структуры, помимо механического измельчения, применяется сопутствующий способ гидрирования (насыщения водородом) исходной шихты с последующим дегидрированием.
Сущность данного способа заключается в том, что, водородонасыщенный титан – весьма хрупкое соединение. Исходное титановое сырье (стружка, губка) подвергают насыщению водородом – гидрированию – до показателей в пределах 338…372 см3 Н2 на 1 г. Ti.
Затем полученный гидрид размалывают до требуемой степени дисперсности, после чего производят обезводороживание путем термовакуумного дегидрирования в температурном режиме 710…810 °С.
В ходе процесса дегидрирования происходит спекание зерен Ti. Для получения готовой продукции спек подвергают измельчению до необходимой консистенции. Контроль гранулометрического состава выполняется путем просеивания измельчаемого спека сквозь сита, ячейки которых имеют определенные размерные параметры. Частицы такого порошка характеризуются осколочной формой. Качество получаемого финишного продукта зависит от чистоты сырья, выход которого, при остаточной насыщенности до 4,22 см3 H2 на 1 г Ti, составляет 92% и более от массового количества исходного гидрида.
В промышленных масштабах способом гидрирования-дегидрирования получают мелкодисперсный порошок Ti фракционного состава (-0,103+0,042) мм. Выход готового продукта превышает 94,89% от массового количества исходного титанового сырья.
Восстановление диоксида титана гидридом кальция
Метод восстановления двуокиси титана (ТiO2) – минерального сырья высокой химической чистоты – в дигидрид титана (TiH2) с последующим разложением его на чистый титан (Ti) и водород (H) имеет широкое практическое применение. СаН2 как восстанавливающий реагент используется благодаря высокой химической активности Са, что делает возможным восстановление подавляющего большинства металлических и неметаллических оксидов безотносительно к их термодинамическим свойствам. При этом СаН2 не образует твердых растворов и других химических соединений с восстанавливаемыми металлами.
В химическом плане реакцию восстановления можно рассматривать как кальциетермический процесс, отображаемый в виде следующей последовательности: TiO2 + 2CaH2-»TiH2+2CaO + H2.
Схема промышленной установки для восстановления ТiН2 из ТiO2 с помощью СаН2 представлена на рис. 4.
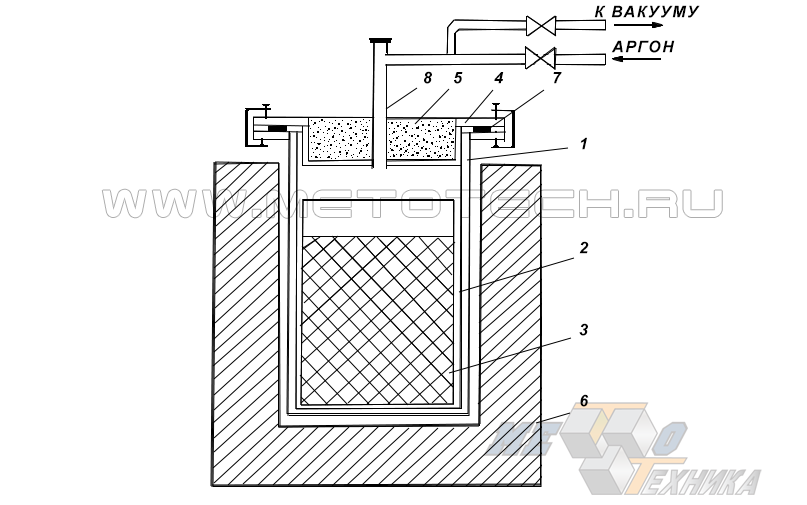
Рисунок 4. Схема установки для восстановления ТiН2 из ТiO2 с помощью СаН2 1 – корпус аппарата (реторта); 2 – стальной тигель; 3 – загружаемая шихта; 4 – крышка; 5 – теплоизолирующая засыпка; 6 – электропечь; 7 – уплотнение; 8 – патрубок для присоединения к вакуум-насосу или источнику Н.
Реакция восстановления осуществляется в вакууме при температуре 900… 1100° С. Исходная порошковая шихта в виде композиции из TiO2 и CaH2 загружается в реторту реактора, изолированную от корпуса печи. После откачки из реторты атмосферного воздуха в нее нагнетают водород высокой очистки, в среде которого происходит восстановительная реакция и остывание полученного продукта после вывода реторты из печи. Остывший спек извлекают, измельчают и выщелачивают из него CaO слабым раствором HCl. После этого оставшийся порошок TiН2 подвергают термическому дегидрированием в вакууме при температуре 700…800°С.
Характеристики порошков марок, произведенных данным способом, отвечают требованиям ТУ 14-22-57-92.
Порошковый Тi, получаемый путем восстановления ТiН2 из ТiO2 с помощью СаН2, характеризуется пористой структурой высокой дисперсности. К сожалению, в его составе велик процент содержания посторонних примесей, а потому без сложной и весьма затратной дополнительной очистки (рафинирования) он малопригоден для промышленного выпуска конструкционной продукции способами порошковой металлургии. Из такого порошка производят различные пористые фильтры-геттеры (газопоглотители) для пищевой и химической промышленности, ряда других промышленных отраслей.
Метод металлотермического восстановления титановых порошков из тетрахлорида титана (TiCl4)
Наиболее востребованным в промышленных целях является т. наз. металлотермический метод изготовления высокочистых титановых порошков из четыреххлористого титана (TiCl4) путем воздействия на него Mg (магниетермия) или Na (натриетермия).
Общая схема процесса представлена на рис. 5.
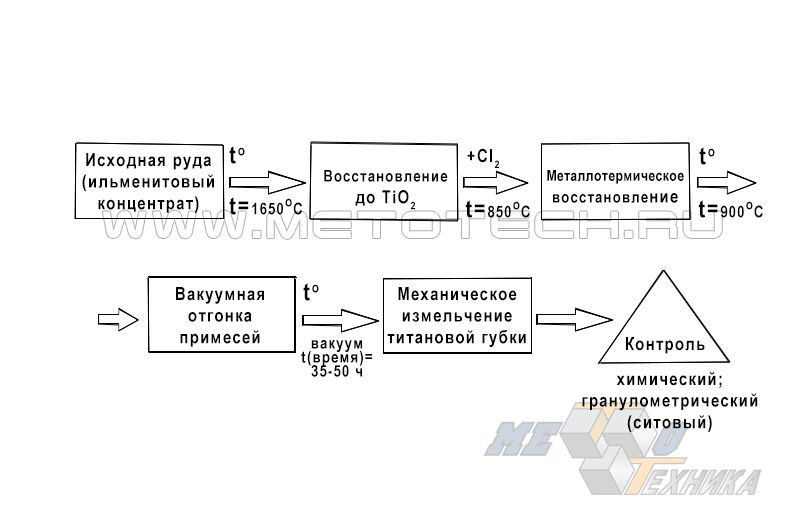
Рисунок 5. Общетехнологическая схема получения порошкового Ti методом металлотермического восстановления TiCl4
В качестве исходного первоначального сырья для осуществления процесса используют ильменитовый концентрат, выделяемый из титаномагнетитовых руд путем их обогащения. Свое название данный продукт получил из-за высокого содержания в нем минерала ильменита (FеО-ТiO2).
Состав концентрата в определенных долях включает:
- двуокись титана ТiO2 – 42...47 %;
- оксид железа (II) FеО – около 30 %;
- оксид железа (III) Fе2О3 – около 20 %.
Технологический цикл восстановления титана из концентрата включает ряд последовательно выполняемых стадий:
- восстановительную плавку концентрата с целью образования шлака, насыщенного двуокисью титана TiO2;
- хлорирование TiO2 для получения тетрахлорида TiCl4;
- металлотермическое восстановление из TiCl4 чистого Ti в виде губки, измельчаемой до порошковой консистенции.
Восстановительная плавка ильменитового концентрата
В ходе данной операции происходит восстановление оксидов железа до чугуна с отделением шлака, насыщенного двуокисью титана TiO2.
Химическая формула реакции:
FeO·TiO2 + С = Fe + TiO2 + CO
Плавка осуществляется в температурном режиме ~ 1650-1700 °С в электродуговых печах (рис. 6), куда загружают исходную измельченную шихту из ильменитового концентрата в смеси с углеродным восстановителем в виде кокса, антрацита или древесного угля.
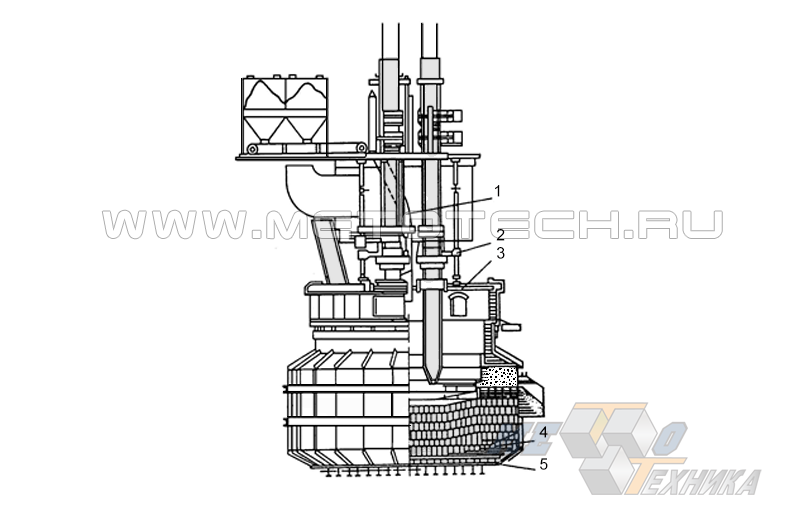
Рисунок 6. Конструкционная схема печи для восстановительной плавки: 1 – подача шихты; 2 – подвод электроэнергии к плавильным электродам; 3 –свод с системой водоохлаждения; 4 – слой магнезитовой футеровки; 5 –печной кожух.
В ходе плавки происходит восстановление насыщаемого углеродом железа с образованием чугуна и шлака, содержащего до 82-92 % диоксида титана (TiO2). Полученный чугун удаляют, а титаносодержащий шлак размалывают и очищают от железосодержащих частиц путем магнитной сепарации, после чего, смешав с определенным количеством мелкого нефтяного кокса, брикетируют. Брикеты обжигают при 710—810 °С и направляют на участок обогащения хлором для получения TiCl4 – исходного сырья для металлотермического восстановления чистого титана.
Получение тетрахлорида титана (TiCl4) хлорированием TiO2
Тетрахрорид титана (TiCl4) получают, воздействуя на диоксид титана (TiO2) газообразным хлором (Cl) в температурном диапазоне 710…910 °С.
Химическая формула реакции:
TiO2 +2Cl2 + 2С = TiCl4 + 2СО.
Существует две основных промышленных технологии хлорирования TiO2 с переходом в TiCl4, различия которых обусловлены типом применяемого реактора-хлоратора. Наиболее распространенной является технология с использованием электропечей-реакторов шахтного типа.
Востребованным являются также метод обогащения хлором двуокиси титана в расплаве солей (КС1, NaCl, CаСl2, МgСl2) с применением специальных солевых хлораторов.
Хлорирование в шахтных хлораторах
В электродуговую печь загружают брикеты исходной шихты, спрессованные из титансодержащего шлака и нефтяного кокса, которые насыщают газообразным хлором в режиме высоких температур. Интенсивность, а значит, и продолжительность реакции определяется температурой процесса, размерными характеристиками брикетов, процентным составом ингредиентов (шлак с TiO2 + нефтекокс), степенью их дисперсности, показателями пористости и некоторыми другими факторами.
Процесс, имеющий гетерогенный характер, включает в себя три условных технологических цикла:
- нагнетание Cl к шихтовой массе;
- диффузионное проникновение Cl в тело брикета;
- непосредственно процесс реакции.
Характеристики первого цикла определяются особенностями динамики газового потока. Насыщение брикета Cl, а значит, и сама реакция, протекает постепенно, с образованием хлорируемой зоны, ограниченной по протяженности и постепенно смещающейся от поверхностного слоя вглубь брикета, к его центру, оставляя за собой непрохлорированный «огарок».
Глубина хлорируемой зоны определяется температурным критерием: уже при 410-460 °С она превышает радиус брикета, обеспечивая непрерывность насыщения его пор хлором по всему объему (кинетическая зона). С дальнейшим наращиванием температуры коэффициент интенсивности реакции начинает превышать константу диффузии газов, вследствие чего происходит смещение вектора процесса в переходную, а затем в диффузионную зону.
На рисунке… представлено схематической изображение шахтной электропечи (ШЭП) с полунепрерывным принципом функционирования.
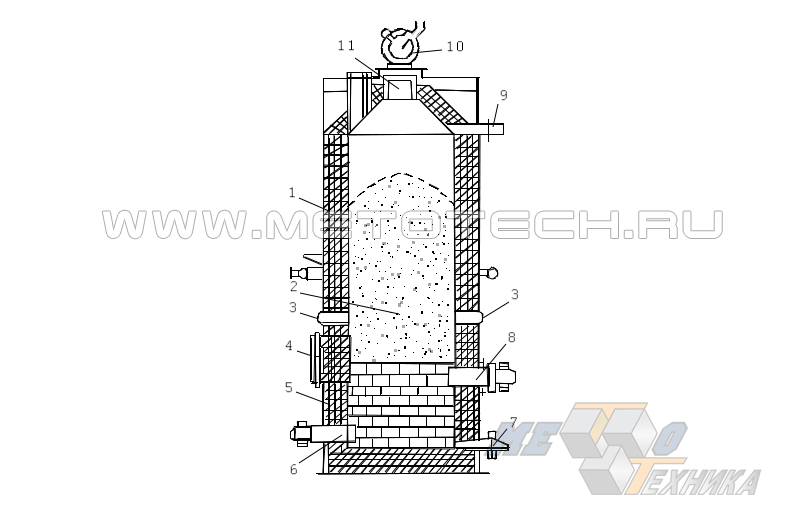
Рисунок 7. Схема шахтной электропечи (ШЭП) полунепрерывного действия: 1 — футеровочный слой; 2 — брикетированная шихта; 3 — патрубки подвода хлора; 4 — смотровая отдушина;5 — слой графитоугольной набивки;6 — нижние электроды; 7 — летка; 8 — верхние электроды; 9 – труба для отведения парогазовой смеси; 10 — питатель золотникового типа; 11 - загрузочный колодец.
Нижнюю зону футерованной (1) печи заполняют графитоугольной набивкой (5), разогреваемой сверху и снизу (6,8) электродами до ~ 710 °С, что обеспечивает поддержание в расплавленном виде образуемых высококипящих хлоридов Mg, Ca и Fe.
На графитоугольную набивку сквозь отверстие загрузочного колодца (11) через питатель золотникового типа (10) засыпается брикетированная шихта (2), сквозь которую пропускают поток подогретого хлора (3). Хлор интенсивно реагирует почти со всем объемом шихты (остаточное содержание – не более 0,01% общей массы). В ходе экзотермической реакции температура в хлорируемой зоне возрастает до ~ 1150 °С.
Основные продукты реакции (тетрахлорид Ti в смеси с небольшим количеством примесей хлоридов Al, Fe, V, Si и др.) переходят в газообразное состояние. Образующуюся парогазовую смесь выводят из реактора сквозь специальную трубу в его верхней зоне (9), после чего направляют на конденсацию и дополнительную очистку от примесей. Соотношение СО2 : СО в парогазовой смеси на выходе из выводной трубы варьируется в диапазоне 1,01 : 5,01÷8,01. Такая смесь в соединении с кислородом взрывоопасна: во избежание подсоса воздуха в реакторной емкости поддерживают режим избыточного давления. Степень перехода TiO2 в TiCl4 очень высока, достигая 99 %. Оставшийся непрохлорированный шлак периодически выгружается сквозь летку в нижней части печи (7).
Хлорирование в расплаве солей
Процесс получения TiCl4 путем насыщения TiO2 хлором в расплавах солей также находит промышленное применение. На рисунке… приведено схематическое изображение реактора, действующего по данному принципу.
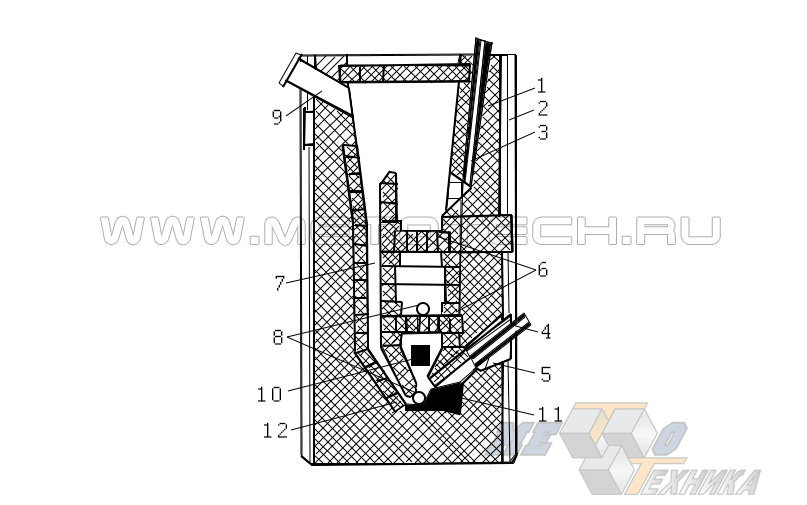
Рисунок 8. Солевой хлоратор (схема) 1 — реакторная емкость; 2 — внешний контур; 3 — канал засыпки шихты; 4 — подача хлора; 5 — фурма (нагнетательное устройство); 6 — распределительные решетки; 7 — тракт циркуляции парогазовой смеси; 8 — летки для удаления непрохлорированного остатка; 9 — труба, отводящая парогазовую смесь; 10 — электрод из графита; 11 — графитовая подина; 12 — футеровочный слой.
Процесс хлорирования протекает в реакторной реторте, заполняемой солевым расплавом (КС1, NaCl, CаСl2, МgСl2).
Измельченная шихта из насыщенной TiO2 шлаковой составляющей в смеси с нефтекоксом засыпается на поверхностный слой расплава сквозь загрузочный канал-течку (3). В нижнюю часть реторты под давлением нагнетается хлор (4, 5), вследствие чего происходит бурная циркуляция расплава с выделением и отводом (7, 9) СО2 и СО, концентрация которых не превышает 4,5 % общего объема. Нагнетаемый хлор вступает в реакцию со слоем шихты, равномерно размещенной по всей площади распределительных решеток (6). Температурный диапазон протекания реакции – 740-820 °С.
Металлотермическое восстановление Ti из ТiСl4 при помощи Mg и Na
Восстановление титана из тетрахлорида ТiСl4 металлотермическим способом (рис. 9) осуществляется с использованием Mg (магниетермия) или Na (натриетермия).

Рисунок 9. Промышленная линия металлотермического восстановления Ті из ТiСl4
При этом магниетермия и натриетермия, при общей схожести технологических операций, обладает своими достоинствами и недостатками.
Восстановление магнием (магниетермия)
Для магнийтермического восстановления применяют установку (рис. 10), состоящую из печи и помещаемой в ее корпус герметичной реторты из хромоникелевой стали. Реторту разогревают до ~ 760 °С, после чего в нее загружают измельченный ТiСl4, заливаемый расплавом Mg.
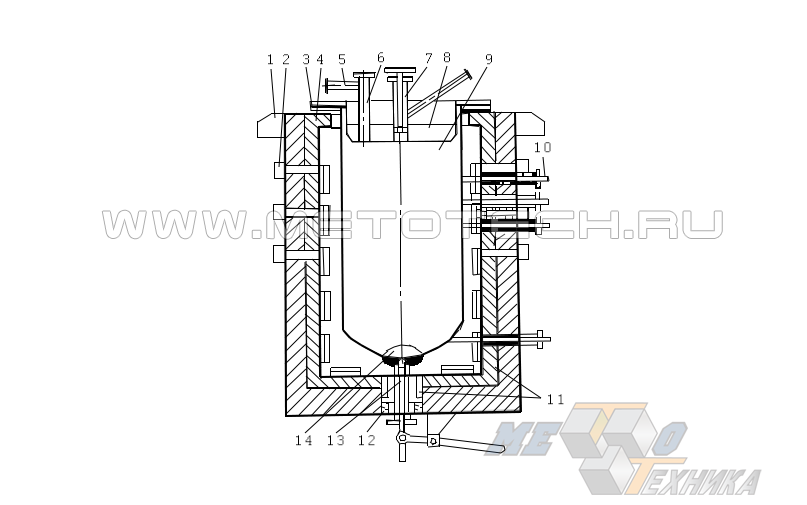
Рисунок 10. Схема установки для магнийтермического восстановления Ті из ТiСl4: 1 – опорная плоскость печи; 2 – коллекторы нагнетания/откачки воздуха; 3 –соединительный фланец с водоохлаждением; 4 – футеровочный слой; 5 – патрубок со штуцером для вакуумирования и нагнетания инертного газа (Ar);6 – колодец заливки Mg; 7 – колодец подачи TiCl4; 8 – крышка реторты; 9 – емкость реторты; 10 – термощупы контактного типа; 11 – термоэлектроды; 12 – песчаный затвор; 13 – шток слива; 14 – псевдоднище.
Основная реакция процесса (TiCl4 + 2Mg = Ti + 2MgCl2), являясь экзотермической, протекает с выделением тепла, вследствие чего функцию электронагрева периодически приостанавливают, охлаждая реторту воздушной струей для соблюдения температурного режима, не выходящего за пределы 810…910 °С. Регуляция температуры возможна также за счет изменения интенсивности подачи TiCl4. Продолжительность восстановительного цикла может составлять 32-52 ч. За это время в реторте формируется губчатый титановый спек. Пребывающий в жидком состоянии MgCl2 откачивают из реторты, не прерывая процесса.
Титановый губчатый спек вбирает в себя большое количество MgCl2 и Mg. В связи с этим по завершении восстановительного цикла производят вакуумную отгонку примесей. Реторта после разогрева до ~ 1050 °С и создания в герметичной емкости вакуумного разрежения постепенно остывает в на протяжении 38-58 ч. до полного испарения примесей. В ряде случаев удаление примесей из губчатого спека производится уже после его извлечения из реторты. Удаление из реторты блока спеченной титановой губки выполняют, используя для этого гидравлический пресс.
После извлечения блок губки разделяют на неочищенный титановый губчатый спек (крицу) и шлаковый гарнисажный слой. Гарнисаж сразу же удаляют, а крицу очищают механическим способом с применением пресса, отделяя контактирующий с решеткой поверхностный слой на толщину 1,5-2 см, до обнажения чистого металла. После этого с поверхности крицы посредством пневмозубила отделяют остаточные загрязнения. Далее очищенную крицу перерабатывают на прессе, способном выполнять предварительную послойную резку. Срезанный с верхушки блока крицы слой губчатого Ti (примерно четвертая часть общей толщины блока) измельчают в шаровой мельнице, после чего подвергают рассеиванию по фракциям на барабанных грохотах. Затем цикл очистки повторяют по отношению к каждому последующему слою блока крицы.
Каждая партия конечного продукта (порошковый Ti) комплектуется из определенной фракции с проведением химанализа на процентное содержание Ni, Cr, Fe и других включений сообразно требованиями к марке титанового порошка.
Восстановление натрием (натриетермия)
Принцип восстановления Ti с помощью Na во многом схож с магниетермией, что обуславливает и общность конструкции применяемых промышленных установок.
В емкость реакторной реторты подается TiCl4 и жидкий натрий.
Реакция восстановления протекает по формуле: TiCl4 + 4Na = Ti + 4NaCl.
Высокотемпературный режим (810-890 °С) поддерживается благодаря экзотермическому характеру реакции, протекающей с выделением тепла. Получаемый губчатый спек содержит 17,5 % Ti и 82,5 % NaCl. После извлечения из корпуса реактора монолитный спеченный блок подвергают измельчению и операции выщелачивания NaCl, после чего остаток в виде чистого Ti размалывают в мелкодисперсный порошок для товарной расфасовки.
Сравнение магниетермического и натриетермического способов восстановления Ti из TiCl
Химсостав титанового порошка, изготовленного методом магниетермии, характеризуется такими параметрами:
- 0,015-0,55 % Mg;
- ~0,072 % Cl;
- ~0,11 % Н;
- 0,014-0,048 % N;
- 0,032-0,041 % С.
- Остальное – чистый Ti.
Подвергая спрессованный в брикеты порошок последующим циклам прогрева и вакуумного спекания в среде инертного газа (Ar) при 1055°С возможно понизить содержание Mg и Н до сотых и даже тысячных долей процента с сопутствующим возрастанием чистоты Ti до 99,6—99,8 %. Что касается Cl и N, то их можно полностью удалить, подвергнув порошок дополнительной переплавке.
Несомненным достоинством натриетермии является намного более низкая, в сравнении с Mg, Т° плавления Nа (соответственно, 650 и 97,8 °С), что весьма упрощает процессы очистки и подачи в реактор жидкого Nа. Однако количество теплоты, выделяемой при натриетермии, на 72% превышает аналогичный параметр магниетермического процесса, что обуславливает необходимость дополнительных энергозатрат на принудительное охлаждение (примерно на 25% выше в сравнении с магниетермией) и ограничивает возможность протекания процесса с высокой скоростью (удельная производительность реакторов при натриетермии ниже по сравнению с магниетермией). Кроме того, по качеству натриетермический Ti значительно уступает металлу, полученному магнийтермическим способом.
Результаты приведенного выше сопоставления, в общем и целом, свидетельствуют в пользу магниетермии, поэтому данный способ восстановления титана востребован гораздо шире, чем натриетермический. Вместе с тем, в ряде ситуаций натриетермия оказывается единственно возможным вариантом получения порошкового титана с требуемыми функциональными характеристиками.
Получение высокочистых порошков Ti электролитическим разложением тетрафторида TiF4
В отличие от металлотермического восстановления, метод получения Ti из TiF4 основан на разложении четырехфтористого титана с применением электролиза без необходимости использовать дорогостоящий металл-восстановитель.
Общее описание техпроцесса
Процесс происходит поэтапно в рамках схемы, изображенной на рис. 11.
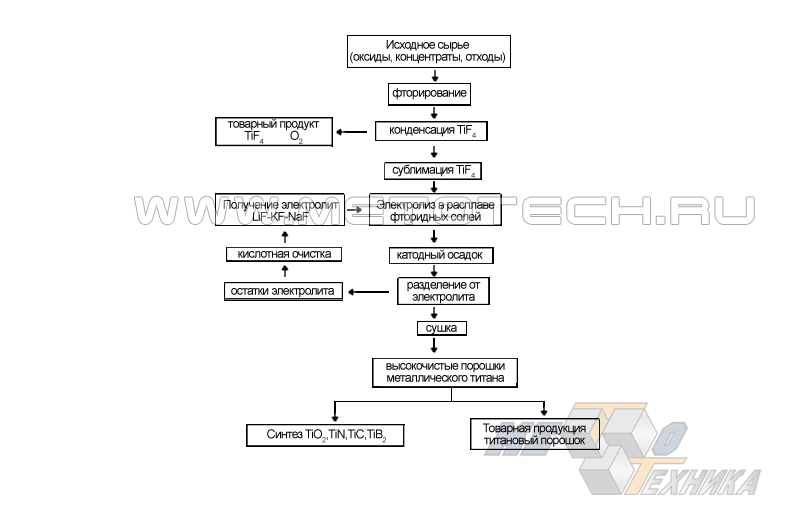
Рисунок 11. Схема получения чистого порошкового Ti путем электролиза TiF4
На первоначальной стадии получают востребованный для электролитического разложения TiF4 из подвергаемых фторированию исходных титаносодержащих материалов (гл. обр. в виде диоксида TiO2, а также концентратов, отходов и т.д.).
Химическая реакция фторирования TiO2 протекает по формуле: TiO2 + 2F2 → TiF4 + O2.
При этом реагирование, вследствие экзотермического характера реакции, происходит с выделением тепла и саморазогревом реагентов до 310-360 °С. На выходе образуется газообразная композиция, состоящая из смеси паров тетрафторида титана (95,5-98,2 % объема исходного сырья) и кислорода. TiF4 отделяют от O2 путем конденсации, а затем, после откачки кислорода и очистки от нелетучих примесей, чистый конденсат вновь сублимируют в газообразную фазу.
Основная стадия общетехнологического процесса осуществляется в аппарате-электролизере и предусматривает непосредственно электролитическое получение металлического Ti из TiF4 в предварительно подготовленном расплаве электролита-флинака.
Флинак представляет собой относительно низкоплавкую (Тпл=473 °C) эвтектическую смесь фторидных солей щелочных металлов (0,51 М LiF - 0,38 М KF- 0,11 М NaF). Электролиз осуществляется в вакууме, в среде инертного газа. После расплавления флинака из электролизера откачивают воздух, заполняют емкость аргоном и герметизируют.
Газообразный сублимат TiF4 порционно направляют в расплавленную фторидную эвтектику, насыщение которой происходит с выделением большого количества тепла и образованием комплексной соли: TiF4(г)+KF(LiF, NaF)(ж) = K2(Li, Na)2TiF6(ж)
Подача на электроды электролизера постоянного тока сопровождается следующими процессами:
- на катоде образуется осадок в виде механической смеси частиц чистого Ti и компонентов электролита (Ti4++ 4е → Ti °);
- на аноде выделяется газообразный фтор (4F- - 4е → 2F2 °).
Катодный осадок периодически счищают и собирают в приемной емкости, являющейся составной частью электролизера. Выделяющиеся на аноде и скапливающиеся в верхней части аппарата пары фтора очищают от аэрозольных примесей и направляют на регенерацию, после чего возвращают в цикл.
На завершающей стадии скопившийся в приемной емкости электролизера катодный осадок извлекают и вымывают из него посторонние включения, после чего порошок чистого Ti сушат и расфасовывают.
Получаемый порошок титановый электролитический (ПТЭ) имеет высокую чистоту и может применяться с целью изготовления фильтрующих элементов и газопоглощающих геттеров (рис. 12).

Рисунок 12. Геттеры из электролитического титанового порошка
Использование ПТЭ практикуется также для нужд порошковой металлургии (в т.ч. синтез оксидов, карбидов, боридов, нитридов, гидридов и других соединений титана).
Преимущества метода
- Порошок титана электролитический (ПТЭ), получаемый описанным выше способом, является высокочистым сырьем, не подлежащим, в отличие от губки, дополнительному измельчению и рафинированию – операциям сложным и весьма затратным.
- Процесс протекает по замкнутому циклу без использования восстановителей из дорогостоящих металлов (Mg, Na, Ca и др.).
- Гибкая технология позволяет использовать различное титансодержащее исходное сырье и быстро переходить с одной его разновидности на другую.
- Применение электролита в виде низкоплавкой солевой эвтектики обеспечивает снижение температурного диапазона с сопутствующим энергосбережением.
Кроме того, к числу достоинств метода можно отнести:
- пожаро- взрывобезопасность;
- экологичность;
- высокую производительность оборудования;
- возможность максимально автоматизировать производственные процессы на всех этапах общетехнологического цикла.
Сумма перечисленных преимуществ обеспечивает возможность минимизировать себестоимость конечного продукта, а значит, предельно расширить сферу его практического применения.
Получение высокочистого Ti методом электротермического йодидного рафинирования титанового сырья, загрязненного примесями
В основу данной технологии заложен принцип термической диссоциации газообразного йодида TiI4 на поверхности накаляемой электротоком до высокой температуры (1301…1501 °C) титановой проволоки. К сожалению, на сегодняшний день ее применение позволяет получать высокочистый титан лишь малыми партиями.
Сущность метода йодидной очистки Ti от примесей O, N, C состоит в том, что подавляющее большинство оксидов, нитридов и карбидов нейтральны по отношению к йоду, не вступая во взаимодействие с этим химическим элементом. В ходе процесса рафинирования устраняются также примеси металлов, которые не образуют летучих йодидов.
На рис. 13 представлена схема установки для электротермического йодидного рафинирования Ti. Корпус аппарата выполнен из не подверженного воздействию паров йода сплава Ni (82 %) и Сг (18 %),.
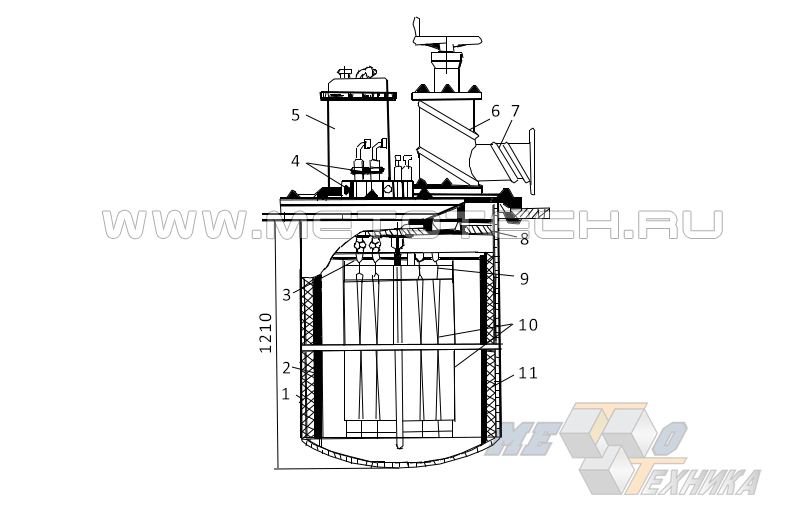
Рисунок 13. Установка для электротермического йодидного рафинирования Ti:
- 1 – внешняя оболочка;
- 2 – сетчатая стенка из Мо, формирующая кольцевую полость для загрузки исходного титанового сырья;
- 3 – площадка для подвешивания титановых нитей;
- 4 – токоподводящие молибденовые электроды;
- 5 – корпус термостата, содержащего ампулу с йодом;
- 6 – затворно-вакуумное устройство;
- 7 – труба откачки воздуха для создания вакуума;
- 8 – крышка реактора;
- 9 – крючки из Мо, на которые подвешиваются отрезки титановой проволоки;
- 10 – отрезки проволоки из Ti, последовательно соединенные общим молибденовым проводником;
- 11 – загружаемое в аппарат исходное титановое сырье.
Исходное титановое сырье в виде крупнозернистого порошка, мелкой стружки или губки располагают в кольцевой полости между внешней оболочкой аппарата и параллельно расположенным экраном сетки из молибдена, не вступающего в реакцию с йодом и йодидами Ti.
В центральной части реактора на специальных молибденовых крючках-подвесах натянуты шесть прямых двухметровых стержней из титановой проволоки (Ø 2,5-3,5 мм), последовательно соединенных между собой молибденовым проводником и образующих, таким образом, единую цепь общей длиной 12 м.
Верхние концы крайних стержней подсоединены к молибденовым токоподводящим электродам. К корпусу реактора примыкает термостат, осуществляющий поддержание заданного температурного режима в полости с титановым сырьем (в диапазоне 100,1…200,1 °С). Внутри термостата размещается стеклянная ампула с йодом.
Сначала из реторты реактора откачивают воздух до создания необходимого вакуумного разрежения. Затем, раздавливая ампулу, впускают в реактор йод и подают на проволоку электрический ток, раскаляющий ее до 1301…1501 °C. Количество йода составляет около 7,1-10,1 % от массы загружаемого титанового сырья.
Технологический цикл характеризуется трехэтапным течением в рамках общехимической схемы: Ti(исходный)+ 2I2(пар)→TiI4(пар) →Ti(чистый)+ 2I2(пар).
- Исходный Ti (загрязненный примесями O, N, C и, в меньшей концентрации, других химических элементов), взаимодействует с парами йода при относительно низкой температуре (100,1…200,1 °С), образуя газообразный TiI4.
- Данное промежуточное соединение, беспрепятственно проникая в реактор сквозь поры сетчатого экрана, диссоциирует на нагретой до 1301…1501 °C поверхности проволоки, в результате чего на поверхности стержней равномерно осаждается чистый кристаллический Ti, образуя прутки.
- Высвобождающийся при этом газообразный йод вновь вступает в реакцию с исходным титановым сырьем, находящимся в кольцевидной емкости аппарата, при поддерживаемой термостатом низкой температуре (100,1…200,1 °С). Оптимальное протекание реакции делает возможным увеличение Ø прутка на 10,1-20,1 мм/сут.
Процесс характеризуется непрерывным течением и продолжается до полной выработки из исходного сырья чистого Ti (99,55-99,98 %). Образующийся в полости осадок (смесь не вступающих в реакцию с йодом посторонних примесей) по завершении цикла удаляют.
В результате рафинирования получают прутки чистого Ti плотной мелкозернистой кристаллической структуры (Ø 25,1-40,1 мм). Концентрация примесей в очищенном металле на несколько порядков ниже, чем в металле, получаемом металлотермическим восстановлением TiCl4.
Получаемый чистый Ti содержит (%):
- О – 0,0031-0,0051;
- N – 0,0011-0,0041;
- С – 0,011-0,031.
Содержание металлических примесей не превышает сотых долей процента.
Установка обеспечивает возможность получения 24,1 кг чистого Ti за полный цикл или около 10,1 кг в течение суток. Малая производительность в сочетании с высокой себестоимостью получаемой продукции – единственный, хотя и весьма существенный недостаток, ограничивающий возможность производства особо чистого титана данным способом в промышленных масштабах.
Практическое применение титановых порошков
На протяжении последних десятилетий порошковые технологии металлургии титана развивались революционными темпами. Промышленная продукция из порошкового титана вобрала в себя весь комплекс полезных свойств, присущих компактному металлу, включая невысокую плотность, прочность, устойчивость к коррозии и воздействию агрессивных сред, немагнитность, биоинертность и т.д.
Порошки Ti и сплавов находят применение:
- для изготовления коррозиеустойчивых пористых фильтрующих элементов, позволяющих выполнять тонкую очистку жидкого топлива;
- в производстве регенерируемых фильтрующих элементов для пищевой промышленности;
- для выпуска газосорбционных геттеров, имеющих высокую поглощающую способность и значительную емкость;
- в медицинской и ортопедической отраслях для получения легких физиологически нейтральных имплантатов, протезов самых разных органов, хирургического инструментария, приборов и т.д.;
- для изготовления высоконадежной пиротехники;
- в производстве металлических и неметаллических композитных материалов;
- для изготовления часов и ювелирных украшений (рис…);
- в производстве оборудования, устойчивого к воздействию кислотных сред;
- для напыления износоустойчивых покрытий на металлические и полимерные поверхности;
- для изготовления лопаток турбин, лопастей гребных и воздушных винтов, других ответственных деталей машин и механизмов.
Сегодня множество изделий, для изготовления которых ранее применялся только монолитный титан, успешно изготавливают из титановых порошков. Порошковый титан прекрасно прессуется, будучи засыпанным как в жесткие пресс-формы, так и в эластичные оболочки (т. наз. гидростатическое прессование), отлично спекается в условиях вакуума и среды инертных газов (аргон и др.). Упомянутые технологии, в отличие от механической обработки компактного металла, являются безотходными, позволяя свести к минимуму себестоимость конечной продукции.
Порошки титановые химические (ПТХ), изготавливаемые способами металлотермического восстановления, характеризуются высокой стойкостью в агрессивных средах. Они широко используются в гидрометаллургии цветных металлов, а также в химическом машиностроении для создания защитных пленок, наносимых путем плазменного напыления на поверхности корпусов химических реакторов и другого оборудования.
Титановые порошки в смеси с эпоксидными смолами применяют для изготовления антикоррозийных композиций, наносимых на подводную часть корпусов морских судов. Из подобных составов формируют также защитные покрытия для гальванических ванн, подверженных воздействию кислотных, щелочных, бензоловых и других агрессивных сред в химико-металлургической, нефтехимической, фармацевтической и других производственных отраслях.
Порошковый титан составляет 4–7 % массы покрытия сварочных электродов (рис. 14), используемых в дуговой сварке (мас. %: рутила – 35, криолита – 16, мрамора – 14,5, алюминия – 8, прочее – фториды Na и Ca, а также силикаты).

Рисунок 14. Сварочные электроды с титановым покрытием
Введение 7–11 % порошкового Ti в смесь, включающую нефтекокс (73–81 %), графит и каменноугольный спек, повышает степень термостойкости материала.
Гранулированный титан является исходным материалом для изготовления различных изделий с применением такого современного метода, как селективный лазерный синтез. В частности, гранулы титана и его сплавов широко используются для изготовления лопаток турбин электростанций и воздушно-реактивных двигателей по технологиям горячего изостатического прессования ГИП (рис. 15).

Рисунок 15. Лопатки турбины, изготовленные из титанового порошка по технологии «ГИП + деформация»
Метод ГИП предусматривает формование заключенной в эластичную оболочку порошковой заготовки с ее одновременным нагревом до высокой температуры, вследствие чего процессы пластической деформации и спекания происходят под воздействием давления, равномерного по всем направлениям. Изделия, изготавливаемые по технологии «ГИП+деформация», отличаются высочайшей прочностью и надежностью.
Таким образом, титановые порошки – перспективное сырье, которое с течением времени будет все шире использоваться для нужд множества отраслей в гражданской и военной сфере.
Порошки титана в аддитивных технологиях (3D печать)
Сущность и преимущества аддитивных технологий
Аддитивными технологиями (Additive Manufacturing) называют методы синтеза материальных объектов их послойным наращиванием при помощи компьютерной 3D-печати.
Одними из самых распространенных расходных материалов для лазерных 3D-принтеров являются металлические порошки. Их применение позволяет объединить в себе главные преимущества таких методов получения изделий, как порошковая металлургия и литейное производство.
Сегодня 3D-печать металлом считают одной из самых прогрессивных технологий, уже в ближайшем будущем способной прийти на смену методу механообработки. Применение металлорежущих станков утрачивает былую актуальность еще и потому, что в ходе 3D-печати не образуется непродуктивных отходов в виде опилок, стружки и т.п.
Использование 3D-принтера (рис. 16) делает возможным изготовление деталей такого уровня сложности, которую традиционные обрабатывающие центры достичь не в состоянии.

Рисунок 16. Современный промышленный 3D принтер
Кроме того, 3D-печатный процесс способен обеспечивать выход деталей, скомпонованных из различных материалов, доселе считавшихся абсолютно несовместимыми. Таким образом, печатать можно как отдельные фрагменты, так и целостные изделия – смартфоны, автомашины, многоэтажные здания со всеми бытовыми коммуникациями, а также более масштабные инженерные конструкции.
Значение титановых порошков для аддитивных технологий
Титановые порошки особенно перспективны для использования в аддитивных технологиях. Их важнейшие преимущества заключаются в низкой плотности, способности не утрачивать функциональности при высоких температурах и устойчивость к коррозии даже в экстремальных условиях.
Наиболее промышленно востребован для EBM-процессов спеченный порошковый сплав Ti6Al4V: сегодня для его получения используется 55-65 % общемировой добычи титана.
Согласно химическим классификациям Ti6Al4V относят к группе α+β-сплавов. Помимо Ti, в его состав входит до 6% Al, и 4% V. Допускается присутствие мелких примесей Fe и O (до 0.27 % и 0.21 % соответственно).
Создаваемые методом 3D-печати изделия из сплава Ti6Al4V характеризуются оптимально высокой плотностью; благодаря мелкозернистой микроструктуре (рис…) они имеют значительно большую прочность в сравнении с литыми аналогами.
3D-принтеры и основные способы 3D-печати
3D-принтер — электронно-техническое устройство, позволяющее выполнять пространственную печать различных материальных объектов. Революционность 3D-принтера заключается в том, что он создаёт не плоскую поверхность, а трехмерный пространственный объём.
В основу устройства всех 3D-принтеров, вне зависимости от их конструкции и способов функционирования, заложен единый базовый принцип 3D-печати —целостный объект формируется из тонких горизонтальных слоев расходных материалов (рис. 17).
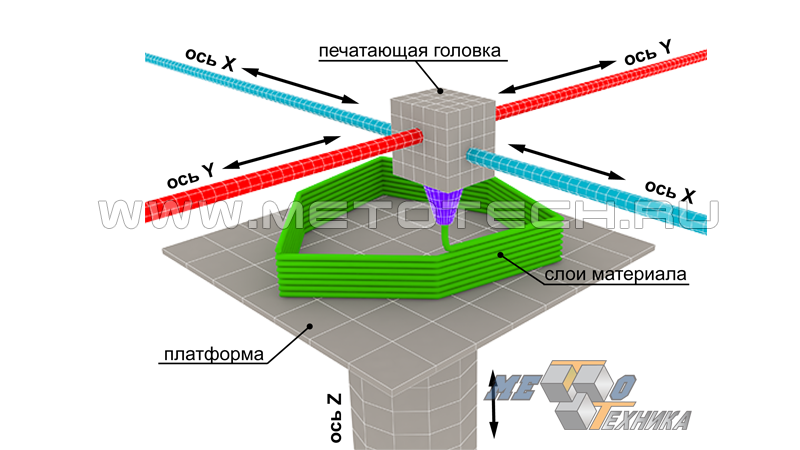
Рисунок 17. Принципиальная схема 3D-принтера
Печатающая головка движется по горизонтальным координатным осям Х и Y, выжимая наносимый материал сквозь фильеру экструдера. При нанесении каждого последующего слоя изменяется значение координаты вертикальной оси Z с опусканием рабочей платформы или поднятием печатающей головки.
Существуют 3D-принтеры различных типовых конструкций, каждая из которых позволяет осуществлять пространственную печать определенным аддитивным методом. Основными из таких методов являются технологии селективного лазерного спекания (SLS) и электронно-лучевой плавки (EBM).
Метод SLS
В последние годы становится все более популярным метод, предусматривающий селективное (выборочное) лазерное спекание, или метод SLS (англ. selective laser sintering).
Схема принципа SLS представлена на рис. 18.
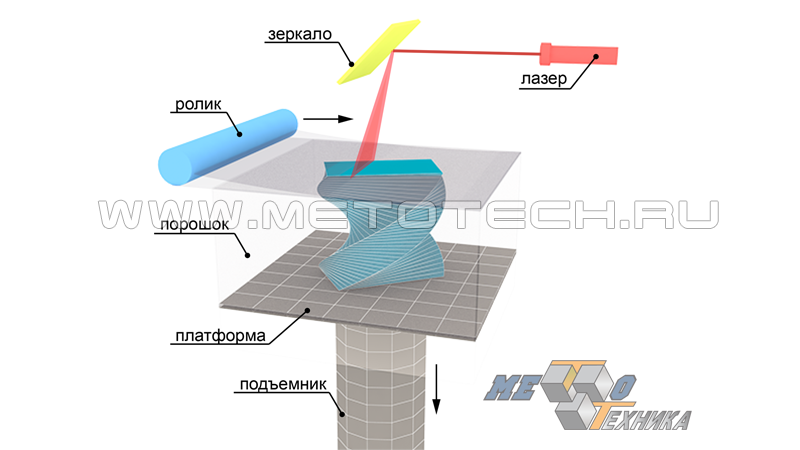
Рисунок 18. Принцип метода SLS
Объект создается послойно. Слои накладываются, начиная от основания и постепенно распространяясь на всю высоту создаваемой модели. Расходным материалом служит определенное количество мелкодисперсного порошка Ti6Al4V. Каждый из напыляемых слоев специальный ролик равномерно распределяет на всю поверхность платформы. После этого при помощи луча мощного углекислотного лазера осуществляется плавка и запекание нанесенного порошкового слоя сообразно заданной программе. По завершении данной операции платформа поднимается: цикл повторяется, в результате чего происходит послойное формирование объекта. Готовую модель подвергают финишной обработке в виде поверхностной полировки до исчезновения следов межслойных переходов.
SLS – один из самых перспективных аддитивных методов: с его помощью можно с одинаковым успехом изготавливать отдельные детали и целостные изделия для машиностроительной, автомобильной и целого ряда других промышленных отраслей (рис. 19).


Рисунок 19. Детали из титанового порошка и колесные диски, полученные методом SLS
Метод EBM
Одной из самых популярных стала 3D-печать способом электронно-лучевой плавки (Electron Beam Melting, сокр. EBM).
Принципиальная схема метода EBM представлена на рис. 20
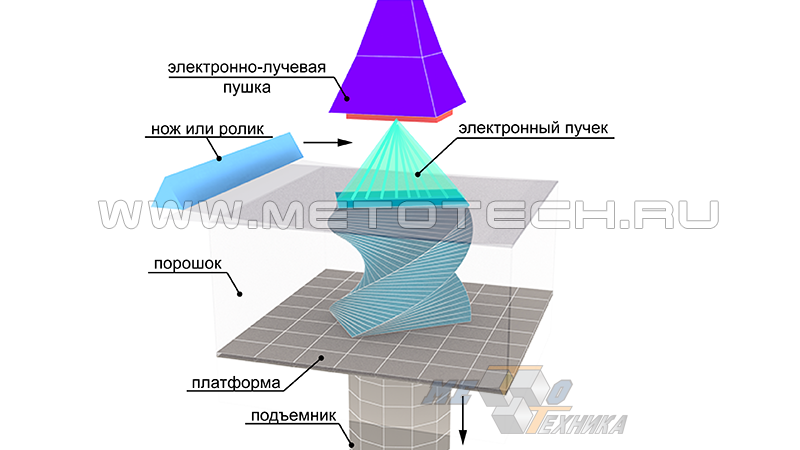
Рисунок 20. Принципиальная схема метода EBM
Конструкционно 3D-принтер для функционирования по методу EBM состоит из нескольких основных компонентов: вакуум-камеры, где создается готовая модель, электронно-лучевой «пушки», формирующей пучок электронов и направляющей его в камеру, подъемника по вертикальной оси, а также блока управления устройством. Расходным материалом служит, главным образом, порошок технического титана марок ТПП или титанового сплава Ti6Al4V.
Перед запуском устройства в вакуум-камеру помещают титановый порошок. Направленный пучок электронов мгновенно плавит металл (температурный режим процесса – 710…1050 °C). Благодаря тому, что электронный луч имеет высокую энергетическую плотность, в камере активизируется процесс разгрузки внутренней напряженности материала, в результате чего достигаются высочайшие показатели прочности. Общий контур модели формируется от слоя к слою. Минимальная толщина каждого слоя составляет 0,051 мм, точность построения модели ± 0,21 мм. После завершения печати и полировки поверхности полученный объект полностью готов к эксплуатации.
Напечатанные методом ЕВМ объекты не нуждаются в дополнительной термообработке и готовы к использованию сразу же после охлаждения до нормальной температуры. При этом все элементы таких объектов характеризуются высокой степенью плотности и отсутствием внутренних пустот. Вот почему конструкционные изделия, создаваемые методом EBM, предназначаются в основном для отраслей, где решающее значение имеют факторы точности, прочности и быстроты изготовления. Это, прежде всего, авиакосмическая и оборонная сфера, а также медицина, в частности, изготовление различных биологически нейтральных эндопропротезов и имплантатов (рис. 21).


Рисунок 21. Фрагмент эндопротеза коленного сустава и полный каркасный протез голени, выполненные из титана методом ЕВМ.
Сферы применения порошков титана в аддитивных технологиях
Применение титановых порошков для использования в аддитивных технологиях является перспективным направлением в развитии различных отраслей промышленности, особенно таких, как прецизионное станкостроение, авиадвигателестроение, возведение строительных объектов, точное приборостроение и др.
Аэрокосмическая отрасль:
- Корпуса и отдельные фрагменты космических аппаратов и реактивных двигателей.
Энергетика:
- Лопатки паротурбин, змеевики теплообменных агрегатов.
Химическая промышленность:
- Сосуды для агрессивных сред.
Производство ГСМ:
- Изделия, стойкие к воздействию углеводородов.
Медицинские отрасли:
- Эндопротезы, имплантаты, хирургический инструментарий, оборудование для инвалидов.
Бытовая сфера:
- Спортивный инвентарь, часовое производство, ювелирные украшения и т.д.
Ближайшими перспективами развития аддитивных технологий является разработка еще более прогрессивных методов 3D-печати с применением титановых порошков.
|
"Метотехника" ® телефоны:
|
|


